Introducción
En este blog hablaremos todo sobre los hidrocarburos aromáticos y los bencenos, todos sus tipos y nomenclatura, también hay un vídeo explicativo que reforzará lo aprendido, al final tenemos unas actividades online para mejorarObjetivos
El objetivo de este blog es entender:- nomenclatura
- orientadores
- Nitracion
- Halogenacin
- Alquilacion
Marco teórico
Los hidrocarburos llamados aromáticos' forman una familia de compuestos que tienen un núcleo común, el núcleo del benceno. Por su estructura cíclica insaturada también se les llama arenos.Su nombre deriva del siglo XIX, cuando se descubrieron varios compuestos que tenían aromas intensos ( bálsamos, esencias, resinas...) y todos tenían el núcleo bencénico.
Así pues, los compuestos aromáticos son derivados sustituidos del benceno o formados por la unión de varios núcleos bencénicos.
El exponente emblemático de la familia de los hidrocarburos aromáticos es el benceno (C6H6), pero existen otros.
La configuración aromático de seis átomos de carbono se denomina núcleo del benceno Los hidrocarburos aromáticos pueden ser monocíclicos o policíclicos.
Estructura
Resonancia del benceno. Cada carbono tiene tres electrones enlazados y el cuarto localizado gira alrededor del anillo.
Una característica de los hidrocarburos aromáticos como el bencenoes es la resonancia, debida a la estructura electrónica de la molécula. Al dibujar el anillo del benceno se le ponen tres enlaces dobles y tres enlaces simples. Dentro del anillo no existen en realidad dobles enlaces conjugados resonantes, sino que la molécula es una mezcla simultánea de todas las estructuras, que contribuyen por igual a la estructura electrónica.
Todos los derivados del benceno, siempre que se mantenga intacto el anillo, se consideran aromáticos. La aromaticidad puede incluso extenderse a sistemas policíclicos, como el naftaleno, antraceno, fenantreno y otros más complejos.
Tipos
Monocíclicos
Monosustituidos
Resultan de la sustitución de un hidrógeno del anillo bencénico por restos hidrocarbonados que se denominan cadenas laterales. En este caso el anillo bencénico se representa como C6H5-, fórmula que corresponde a un benceno que ha perdido un hidrógeno y en cuyo lugar existe otro sustituyente.
Se conocen muchos derivados de sustitución del benceno. Cuando se trata de los compuestos monosustituidos, las posiciones en el anillo bencénico son equivalentes.
Se nombra el sustituyente antes de la palabra benceno.
Nota: Algunos compuestos tienen nombres tradicionales aceptados.
Ejemplos
Metilbenceno o Tolueno(C6H5-CH3)
Vinilbenceno o Estireno(CcH5-CH=CH2)
Etilbenceno
(CcH5-CH2-CH3)
Disustituidos
Cuando el anillo bencénico tiene dos hidrógenos sustituidos sus posiciones relativas se indican mediante números o prefijos. Tomando como ejemplo el dimetilbenceno o xileno.
Se nombran con los términos:
o- (que se lee orto) para la disustitución en posiciones contiguas, 1 y 2 (también sería 1,2-dimetilbenceno);
m- (meta) para las posiciones 1 y 3 (1,3-dimetilbenceno)
y p- (para) para las posiciones 1 y 4 (1,4-dimetilbenceno)
Esquema de la estructura de los diferentes dimetilbencenos C6H4(CH3)2
Polisustituidos
Si hay más de dos grupos en el anillo benceno sus posiciones se deben indicar mediante el uso de números, la numeración del anillo debe ser de modo que los sustituyentes tengan el menor número de posición.
Ejemplos: En el hidrocarburo trisustituido, será 1,2,4-trimetilbenceno (se comienza a numerar el anillo de forma que resulte la combinación de números más baja posible, es decir, 1,2,4- y no 1,3,6- ni 1,4,5-, etc.
1,2,4-trimetilbenceno (C6H3)
1,2,3-trimetilbenceno
Nombre de un compuesto aromático policíclico atendiendo a su nomenclatura
También existen hidrocarburos aromáticos formados por la unión de varios anillos bencénicos (polinucleares) como el naftaleno una de cuyas formas resonantes se ve en la figura 1.
Para nombrar a este tipo de compuestos se indica el número de posición de los sustituyentes, seguido del nombre del sustituyente y seguido del nombre del compuesto.
El orden de numeración de estos compuestos es estricto, no se puede alterar y por ende tienen
nombres específicos.
Compuestos aromáticos policíclicos

naftaleno

antraceno

fenantreno
Reacciones
Halogenacion
El benceno reacciona con halógenos en presencia de ácidos de Lewis para formar derivados halogenados.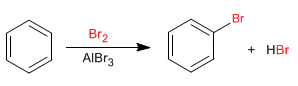
Etapa 1. La molécula de bromo se polariza al interaccionar con el ácido de Lewis. El benceno ataca al bromo polarizado positivamente para formar el catión ciclohexadienilo.
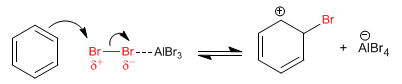
Etapa 2. Recuperación de la aromaticidad por pérdida de un protón.
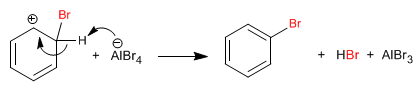
Nitracion
La nitración aromática sucede con compuestos aromáticos gracias a un mecanismo de sustitución electrófila aromática que incluye el ataque de un anillo bencénico rico en electrones por parte del ion nitronio.
El benceno resulta nitrado gracias al reflujo de ácido sulfúrico concentrado y ácido nítrico concentrado a 50 °C.
 2H2SO4 + HNO3 → 2HSO41- + NO2+ + H3O+
2H2SO4 + HNO3 → 2HSO41- + NO2+ + H3O+
C6H6 + NO2+ → C6H5NO2 + H+
H+ + H3O+ + 2HSO41- → H2O + 2H2SO4
El ácido sulfúrico es regenerado y por tanto actúa como catalizador.
Alquilación de Friedel-Crafts

En el caso más simple, implica la reacción entre un haluro de alquilo y una molécula de benceno en presencia de un ácido de Lewis como catalizador. Los productos son alquilbenceno y haluro de hidrógeno.
Ejemplo de alquilación de Friedel-Crafts: reactivos: benceno y clorometano; catalizador: cloruro de aluminio; productos: tolueno y cloruro de hidrógeno
El orden de reactividad aumenta con la polarización del enlace C-X, siguiendo pues el orden RI < RBr < RCl < RF. Habitualmente se usan como catalizadores haluros de aluminio(AlX3) o de hierro (FeX3).
Con haluros primarios (RCH2X) la reacción empieza con la formación del aducto entre el halógeno del haloalcano y el ácido de Lewis: [R-X-AlX3]. Esto provoca la aparición de una carga positiva parcial (δ+) sobre el carbono adyacente al halógeno, lo que hace que sea más electrófilo.
En el caso de haluros secundarios (R2CHX) y terciarios (R3CX) se llegan a formar como intermedios sus carbocationes, junto con el aniónAlX4-.
A continuación una vez generado el electrófilo éste ataca al anillo aromático, seguido de perdida del protón (H+), en forma de HX, y recuperación del catalizador AlX3, según el mecanismo general de una sustitución electrófila aromática.
Practicas
Aqui desarrollaremos lo aprendido:
https://es.educaplay.com/recursos-educativos/1158432-hidrocarburos_aromaticos.html 11



















